 Vytisknout celou knihu
Vytisknout celou knihu
Fyzika atomu
Fyzika atomu
Model atomu
Vývoj názorů na strukturu hmoty
Vnitřní strukturou látky se zabývali jako první starořečtí atomisté - hlavním představitelem je Démokritos (460 - 370 př. n. l.) - na základě filozofických úvah (má-li si látka při postupném dělení zachovávat své vlastnosti, musí existovat hranice tohoto dělení) dospěli k představě atomu - dále již nedělitelné částice hmoty. Atomy různých látek se podle jejich představ liší velikostí a geometrickým tvarem a jsou podle nich odděleny prázdným prostorem. Tato filosofická představa vystačila vědcům téměř 2000 let.
Na počátku 19. století vyslovil svoji atomovou teorii John Dalton na základě zkoumání chemických vlastností látek - atomy nadále považoval za nedělitelné (nestvořitelné a nezničitelné), atomy různých prvků se liší hmotností a velikostí a chemické reakce spočívají v přemísťování atomů.
Nedělitelnost atomu vyvrátil objev elektronu - záporně nabité částice, která se při některých dějích uvolňovala z jinak elektricky neutrální látky (1897, sir Joseph John Thomson). Thomson navrhul model atomu na základě představy rovnoměrně rozprostřené kladně nabité hmoty a v ní rozptýlených záporných elektronů (jako "rozinky v misce anglického pudinku").
Počátkem 20. století dokázal svými pokusy Ernst Rutherford, že naprostá většina hmoty atomu je soustředěna v kladně nabitém jádře nepatrných rozměrů, záporné elektrony obíhají kolem tohoto jádra - tzv. Rutherfordův (planetární) model atomu, v roce 1919 přidal Rutherford do svého modelu představu protonu jako elementární kladně nabité částice, která se nachází v jádře.
Když v roce 1932 objevil James Chadwick v jádře atomu elektricky neutrální částici - neutron, zdálo se, že rodina elementárních částic je úplná.
Dnes víme, že elektron je skutečně elementární částicí, proton a neutron se ale skládají z dalších částic, které se nazývají kvarky (současně přijímaná představa o světě elementárních částic se nazývá Standardní model).
Elektronový obal atomu
Rovněž Rutherfordova představa planetárního modelu atomu se s dalšími objevy zpřesnila (Bohrův model) - elektrony se smí pohybovat kolem jádra pouze v jakýchsi "slupkách", "hladinách" s přesně stanovenou energií, přičemž jednu hodnotu energie smí mít nejvýše dva elektrony (tzv. Pauliho vylučovací princip):
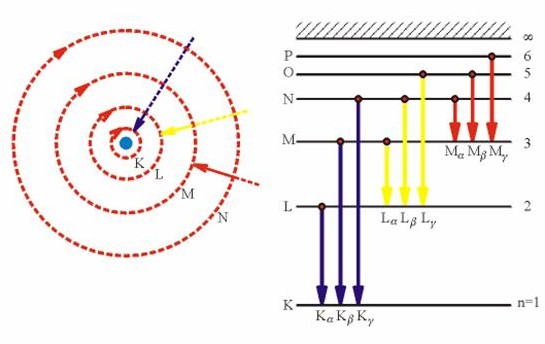
Touto teorií se vysvětluje vznik spekter - fakt, že různé atomy mohou pohlcovat pouze energii určité hodnoty, pohlcená energie se projeví přeskočením elektronu do "vyšší" slupky, při jeho návratu zpět se tato přesně stanovená energie opět vyzáří:
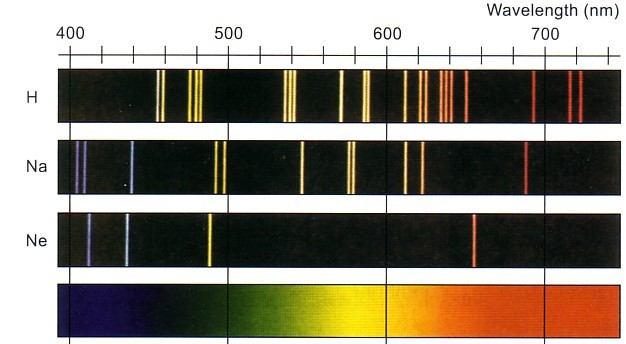
Nukleony, radioaktivita, jaderné záření
Nukleony, stavba atomového jádra
Jádro atomu (jádro=nucleus) zabírá nepatrnou část objemu atomu (uvádí se, že jeho průměr je 1/100 000 průměru atomu), obsahuje však téměř celou jeho hmotu. Je tvořeno kladně nabitými protony a elektricky neutrálními neutrony (dnes víme, že ani tyto částice nejsou základní stavební kameny hmoty, skládají se z tzv. kvarků). Protony a neutrony souhrnně nazýváme nukleony.
K základním vlastnostem částic patří jejich hmotnost, elektrický náboj a doba života. Hmotnost částic se zpravidla udává v násobcích hmotnosti elektronu me, která v absolutních jednotkách činí 9.10-31 kg.
|
Částice
|
Značka
|
Náboj
|
Hmotnost v me
|
Doba života v sekundách
|
| elektron
|
e-
|
záporný
|
1
|
stabilní
|
| proton
|
p+
|
kladný
|
1836
|
asi stabilní
|
| neutron
|
n0
|
neutrální
|
1838
|
900
|
Atomy různých prvků se liší počty částic v jádře a obalu.
Atomy stejného prvku mají v základním stavu stejný počet protonů v jádře a elektronů v obalu - jsou elektricky neutrální. Počet protonů (a elektronů) udává tzv. atomové číslo prvku - v Mendělejevově periodické tabulce jsou prvky podle tohoto čísla řazeny.
Atomy téhož prvku se však mohou lišit počtem neutronů v jádře - hovoříme pak o různých izotopech téhož prvku. Počet neutronů v jádře zjistíme z tzv. nukleonového (hmotnostního) čísla, které udává součet protonů a neutronů v jádře (tak např. 235U představuje izotop uranu s 92 protony - je 92. v periodické tabulce - a 143 neutrony (235=92+143).
Radioaktivita, jaderné záření
Na konci 19. století bylo zjištěno, že jádra atomů některých látek jsou nestabilní a samovolně rozpadají (vznikají jádra jiných prvků, atomy s jinými chemickými vlastnostmi!), přitom se uvolňuje energie v podobě záření. Tento jev se nazývá přirozená radioaktivita a vzniklé záření se nazývá radioaktivní záření - má původ v aktivitě atomových jader.
Radioaktivitu se posléze podařilo vyvolat i uměle ostřelováním jinak stabilních jader různými částicemi.
Dalším zkoumáním bylo zjištěno, že radioaktivní záření má tři složky, které byly označeny prvními písmeny řecké abecedy:
- záření alfa - je tvořeno (kladně nabitými) jádry helia (2 protony + 2 neutony), není nijak pronikavé (uvádí se, že k jeho odstínění sačí list papíru)
- záření beta - je tvořeno (zápornými) elektrony, odstíní jej tenká vrstva kovu
- záření gama - je tvořeno vysoce energetickými (neutrálními) fotony (viz. kapitola Elektromagnetické spektrum), je vysoce pronikavé a živým organismům velmi nebezpečné, k jeho odstínění je třeba silná hmoty, prakticky se používá olovo, beton
Radioaktivní záření je pro živé organismy nebezpečné, má však i řadu praktických aplikací, viz. například www.cez.cz.
Jaderná energie a její využití
Jaderná energie - štěpná reakce
V době těsně před druhou světovou válkou objevili vědci zajímavou věc - pokud se trefíte do jádra uranu 235U volným neutronem, stane se toto jádro nestabilním a rozštěpí se na dvě jádra lehčí. Při tom se uvolní obrovské množství energie (chemickými reakcemi nedosažitelné!) ve formě pohybové (tepelné) energie vzniklých jader a současně vylétnou tři volné neutrony, které mohou způsobit štěpení dalších jader 235U.
Tento objev se dá využít dvěma zcela odlišnými způsoby:
Pokud se nám podaří vyčistit dostatečné množství 235U (tzv. kritické množství), aby vzniklé neutrony nebyly zachyceny "nečistotou" a mohly jako lavina způsobit další a další štěpení, máme základ neřízenou (řetězovou) štěpnou reakci - atomovou (uranovou) bombu.
Pokud se nám podaří "znečistit" 235U právě tak, že dva neutrony budou zachyceny (a další reakci nezpůsobí) a jediný přivede k rozštěpení další jádro 235U, máme základ pro tzv. řízenou štěpnou reakci - atomový reaktor.
Využití jaderné energie
Mírové využití jaderné energie představují jaderné elektrárny:
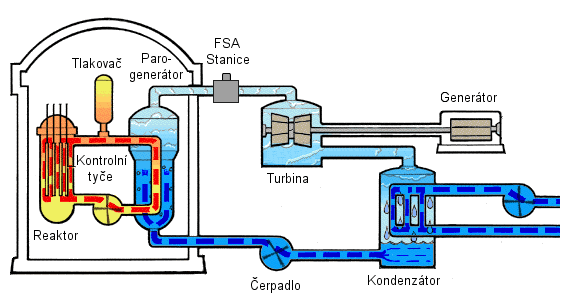
Řízená štěpná reakce probíhá v reaktoru, k jejímu řízení slouží kontrolní tyče, které zachytávají přebytečné neutrony. Teplo, které štěpením vzniká, je předáváno chladicí látce tzv. primárního okruhu - žlutá oblast obrázku (v některých typech reaktorů se k tomuto účelu používají dokonce roztavené soli nebo kovy). Tato látka je vysoce radioaktivní, proto je oddělena od tzv. sekundárního okruhu - modrá/prostřední oblast obrázku, kde v parogenerátoru předá své teplo vodě a přemění ji na páru. Pára pohání turbínu s generátorem elektrického proudu, tím se ochladí a v kondenzátoru je přeměněna zpět na vodu.
Informace o našich jaderných elektrárnách najdete na stránkách www.cez.cz, informace o řešení rizik využití jaderné energie např. zde.
Poznámka - jaderná fúze (slučování jader)
Druhou možností, jak lze získat energii z jaderných reakcí, je přinutit ke sloučení lehká jádra (např. vodíku) na těžší (např. helium). I při takových změnách dochází k uvolňování velkého množství energie (dokonce mnohem většího než u štěpných reakcí!).
Fúzi jako neřízenou reakci lidstvo zvládlo v podobě termonukleárních (vodíkových) bomb.
"Řízená" fúzní reakce probíhá v nitrech hvězd. Pokusy vědců o její napodobení v pozemských podmínkách zatím nejsou ve fázi praktického použití.


